
La Tercera Llei de la Termodinàmica estableix que a mesura que una substància es refreda a una temperatura propera al zero absolut (-273.15°C o 0 Kelvin), la seva entropia, que és una mesura del desordre o la incertesa al sistema, s'aproxima a un valor constant i finit.
Aquesta llei postula que assolir el zero absolut requeriria un nombre infinit de passos, sent inassolible en la pràctica. A més, suggereix que tots els sistemes assolirien un estat de màxima ordre i mínim desordre teòric a aquesta temperatura extrema, cosa que té implicacions fonamentals en camps com la física quàntica i l'estudi de nous materials amb propietats extraordinàries a temperatures ultra baixes.
A continuació es mostren alguns exemples que il·lustren aquest principi:
Exemple 1: Vidres de gel
 Quan l'aigua es refreda a temperatures molt baixes, properes al zero absolut (0 K o -273,15 °C), les molècules d'aigua perden energia cinètica i s'organitzen en una estructura cristal·lina altament ordenada, formant gel. En aquestes condicions, l'energia tèrmica és tan baixa que les molècules gairebé no vibren i adopten una disposició fixa i regular.
Quan l'aigua es refreda a temperatures molt baixes, properes al zero absolut (0 K o -273,15 °C), les molècules d'aigua perden energia cinètica i s'organitzen en una estructura cristal·lina altament ordenada, formant gel. En aquestes condicions, l'energia tèrmica és tan baixa que les molècules gairebé no vibren i adopten una disposició fixa i regular.
A mesura que la temperatura s'acosta al zero absolut, qualsevol desordre tèrmic residual disminueix, i els vidres de gel arriben a un estat d'ordre màxim on l'entropia és mínima. Teòricament, al zero absolut, no hi hauria moviment molecular, i el sistema estaria en el seu estat de menor entropia possible.
Exemple 2: Superconductivitat
La superconductivitat és un fenomen de la física que passa en certs materials quan es refreden per sota una temperatura crítica específica. A aquesta temperatura crítica, els materials superconductors exhibeixen una propietat única: la resistència elèctrica desapareix completament permetent que l'electricitat flueixi sense pèrdua d'energia.
La Tercera Llei de Termodinàmica explica la relació entre la superconductivitat i la reducció de l'entropia a temperatures ultra baixes.
En condicions normals, quan apliquem un corrent elèctric a través d'un conductor, com un filferro de coure, els electrons que transporten l'electricitat s'enfronten a obstacles i xocs amb els ions del material, cosa que genera una resistència al flux d'electrons. Aquesta resistència és la responsable de la pèrdua denergia en forma de calor i limita leficiència dels dispositius elèctrics.
Tot i això, en un material superconductor, a temperatures molt baixes properes al zero absolut, una cosa sorprenent succeeix: els electrons formen "parells de Cooper". Aquests parells estan formats per dos electrons que s'uneixen i es mouen junts a través del vidre sense experimentar resistència.
Exemple 3: Heli líquid
 L'heli és un gas inert a temperatura ambient, però a temperatures extremadament baixes, properes al zero absolut, presenta un comportament fascinant i únic. Quan es refreda prou, aproximadament per sota de 4.2 K, l'heli no se solidifica com a altres gasos, sinó que es converteix en un líquid.
L'heli és un gas inert a temperatura ambient, però a temperatures extremadament baixes, properes al zero absolut, presenta un comportament fascinant i únic. Quan es refreda prou, aproximadament per sota de 4.2 K, l'heli no se solidifica com a altres gasos, sinó que es converteix en un líquid.
A mesura que l'heli es refreda i es converteix en líquid, els àtoms d'heli perden energia tèrmica, cosa que en redueix l'agitació i la mobilitat. Aquesta disminució de l'energia cinètica dels àtoms és una reducció significativa de l'entropia. En temperatures encara més baixes, l'heli exhibeix propietats quàntiques, com la superfluïdesa, on flueix sense cap fricció.
Quan s'acosta al zero absolut, el sistema s'aproxima a un estat d'ordre gairebé perfecte, on l'entropia tendeix al mínim.
Exemple 4: Condensats de Bose-Einstein
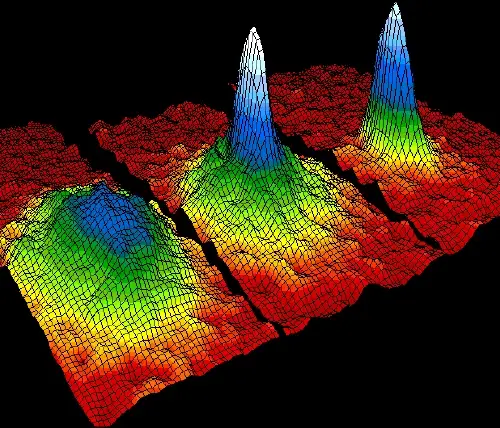 A temperatures properes al zero absolut, alguns àtoms s'uneixen en un estat d'agregació especial anomenat condensat de Bose-Einstein.
A temperatures properes al zero absolut, alguns àtoms s'uneixen en un estat d'agregació especial anomenat condensat de Bose-Einstein.
En aquest estat quàntic, els àtoms perden la seva individualitat i es comporten com una sola entitat quàntica. Aquest fenomen és possible gràcies a la Tercera Llei de la Termodinàmica, que estableix que l'entropia disminueix a mesura que arriben temperatures extremadament baixes.
Aquest fenomen va ser predit per Albert Einstein i el físic indi Satyendra Nath Bose a la dècada de 1920. La idea es basa en l'estadística quàntica de Bose-Einstein, que descriu el comportament de partícules idèntiques i indistingibles, com els fotons de la llum o els àtoms que formen certs elements.
En condicions normals, a temperatures més altes, les partícules segueixen una distribució estadística de Fermi-Dirac (per a fermions) o de Maxwell-Boltzmann (per a bosons).
Tot i això, quan les partícules es refreden a temperatures extremadament baixes, el seu comportament quàntic col·lectiu comença a dominar, i tendeixen a "col·lapsar" en l'estat de menor energia possible. En aquest punt, una gran quantitat de partícules ocupa un sol estat quàntic, formant allò que es coneix com el condensat de Bose-Einstein.
En aquest estat quàntic, les partícules perden la seva individualitat i es comporten com una “superpartícula” col·lectiva, amb propietats quàntiques macroscòpiques. Tota la substància es converteix en una sola entitat quàntica
Exemple 5: Heli sòlid
 A temperatures properes al zero absolut, l'heli líquid també es pot solidificar. En el seu estat sòlid, l'heli exhibeix un comportament inusual, com ara la superfluïdesa, on pot fluir sense resistència a través de capil·lars extremadament estrets, desafiant les lleis clàssiques de la física.
A temperatures properes al zero absolut, l'heli líquid també es pot solidificar. En el seu estat sòlid, l'heli exhibeix un comportament inusual, com ara la superfluïdesa, on pot fluir sense resistència a través de capil·lars extremadament estrets, desafiant les lleis clàssiques de la física.
Exemple 6: Gel sec
 El gel sec és diòxid de carboni (CO₂) en estat sòlid a temperatures molt més baixes que el punt de congelació de laigua. A diferència de l'aigua, que es congela a 0°C, el CO₂ se solidifica directament en forma de gel sec a una temperatura de –78.5°C (-109.3°F) a pressió atmosfèrica normal.
El gel sec és diòxid de carboni (CO₂) en estat sòlid a temperatures molt més baixes que el punt de congelació de laigua. A diferència de l'aigua, que es congela a 0°C, el CO₂ se solidifica directament en forma de gel sec a una temperatura de –78.5°C (-109.3°F) a pressió atmosfèrica normal.
Quan el gel sec es troba a temperatures properes al zero absolut, es comporta de manera similar a altres sòlids a aquestes temperatures extremadament baixes. Les molècules de CO₂ que formen el gel sec redueixen dràsticament la seva energia cinètica, cosa que resulta en una estructura altament ordenada i una disminució significativa de l'entropia. En aquest estat, el gel sec assoliria la màxima ordenació tèrmica possible a temperatura ambient.
El gel sec és àmpliament utilitzat en aplicacions com a refrigerant, a la indústria alimentària, en transport de materials sensibles a la calor i com a efecte especial en el teatre i la indústria de l'entreteniment.